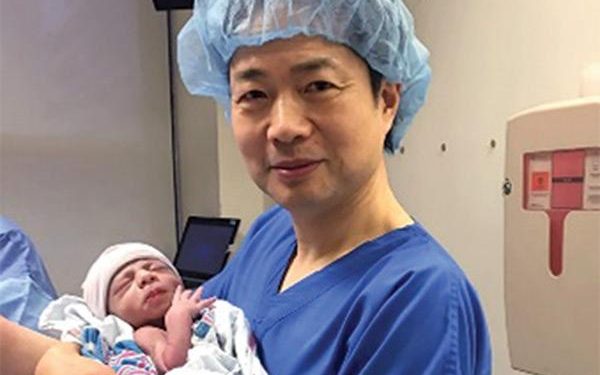
El nacimiento del primer bebé concebido con la ayuda de una nueva técnica experimental con la cual hereda el ADN de tres “padres” diferentes, dos mujeres y un hombre, para evitar que padezca una grave enfermedad, suscita esperanzas pero también plantea preguntas éticas y científicas.
P: ¿Cuál es el objetivo de este método de fecundación?
R: Esta técnica busca eliminar, o minimizar todo lo posible las anomalías de las mitocondrias que originan enfermedades graves que afectan a los músculos, los ojos, el cerebro o el corazón.
Transmitidas exclusivamente por las mujeres, las mitocondrias son “usinas” de energía ubicadas en el seno de las células. Las mismas poseen un ADN mucho menor (apenas 37 genes) que el del núcleo de las células (23.000 genes).
Para el pequeño Abrahim, salido de tres “padres” y nacido en México, se trataba de evitar la transmisión de una enfermedad rara, el síndrome de Leigh, que provoca una degeneración neurológica. Su madre ya había perdido dos hijos, muertos por esta enfermedad.
P: ¿Cómo funciona?
R: Dos técnicas han sido aprobadas en Reino Unido, una a partir del embrión, y la otra a partir del óvulo. Pero hasta ahora ninguna de ellas ha recibido una autorización.
El equipo neoyorquino del Dr. John Zhang, que permitió el nacimiento de Abrahim, utilizó una transferencia de núcleo materno.
Esquemáticamente, esto consiste en extraer el núcleo del óvulo de la futura madre susceptible de transmitir mitocondrias defectuosas, para luego insertarlo en el óvulo ‘desnucleado’ sano de una donante.
De esta manera, el óvulo obtenido es portador de materiel genético de dos mujeres. Inmediatamente es fecundado con el esperma del padre, y luego colocado en el útero de la madre, como en una fecundación ‘in vitro’ clásica.
Al final, el niño habrá heredado el ADN proveniente de dos mujeres y un hombre, aunque el de la donante es minoritario.
Según la American Society for Reproductive Medicine (ASRM), el equipo del Dr. Zhang obtuvo cinco embriones, de los cuales uno sólo era normal, el que se convirtió en Abrahim.
“El método no es perfecto”, señala David Clancy (de la Universidad de Lancaster) puesto que siempre transmitirá un poco del ADN mitocondrial de la madre, afirma.
P: ¿Cuáles son las interrogantes científicas?
R: Es “una nueva esperanza” para las familias afectadas por estas enfermedades devastadoras, según el profesor de genética Darren Griffin (Reino Unido), quien habla de “una nueva era de la genética preimplantatoria”.
Este “primer” nacimiento no ha sido objeto de una publicación detallada en una revista científica de renombre con comité de lectura.
Un publicación de este tipo hubiera permitido responder con rigor a las interrogantes de los especialistas brindando, entre otros, el porcentaje preciso de mitocondrias maternales residuales (portadoras de la enfermedad) que a pesar de todo el niño ha heredado.
Según el equipo de Zhang, “menos del 1%” de las mitocondrias del niño serán portadoras de la anomalía.
Algunos científicos se interrogan sobre el seguimiento a largo plazo del hijo de esta pareja de jordanos.
Muchos juzgan la técnica como “riesgosa” y con “consecuencias imprevisibles” para la salud del niño y sus descendientes, advirtió Marcy Darnovsky, directora del Center for Genetics and Society, una oenegé con sede en California.
P: ¿Y en el plano ético?
R: Algunos, como el Dr. Dusko Ilic, del King’s College de Londres, temen el desarrollo de un “turismo” médico que lleve a los padres a viajar a países con reglas menos estrictas que Reino Unido, por ejemplo, en donde es necesario obtener el aval de la Autoridad británica sobre la fecundación humana (HFEA) para obtener una autorización.
La técnica no está autorizada en Estados Unidos. Trasladarse a México es una manera de eludir estos obstáculos, reprochan algunos.
La obtención de óvulos sin riesgo de apoyarse esencialmente en mujeres desfavorecidas cuya “donación” es remunerada.
Los varones no son transmisores de estas enfermedades mitocondriales, y algunos recomiendan seleccionar por precaución los embriones obtenidos con estas nuevas técnicas y retener solamente los de sexo masculino, una opción que provoca debate.
En los años 1990 hubo un precedente con la inyección de mitocondrias provenientes de una donante para fortalecer a los óvulos de una mujer con dificultades para procrear. Pero, algunos niños luego desarrollaron trastornos genéticos y la práctica fue desechada.
AFP

